#AlMomento
POLICIACA
POLÍTICA
LOCAL
NACIONAL
MUNDO
DEPORTES
ECONOMÍA
OPINIÓN
TEC. Y CIENCIA
ESPECTÁCULOS
SALUD Y BELLEZA
DENUNCIA PÚBLICA
CURIOSAS
 Salud y Belleza
Salud y Belleza| 14 de Octubre, 2023 |
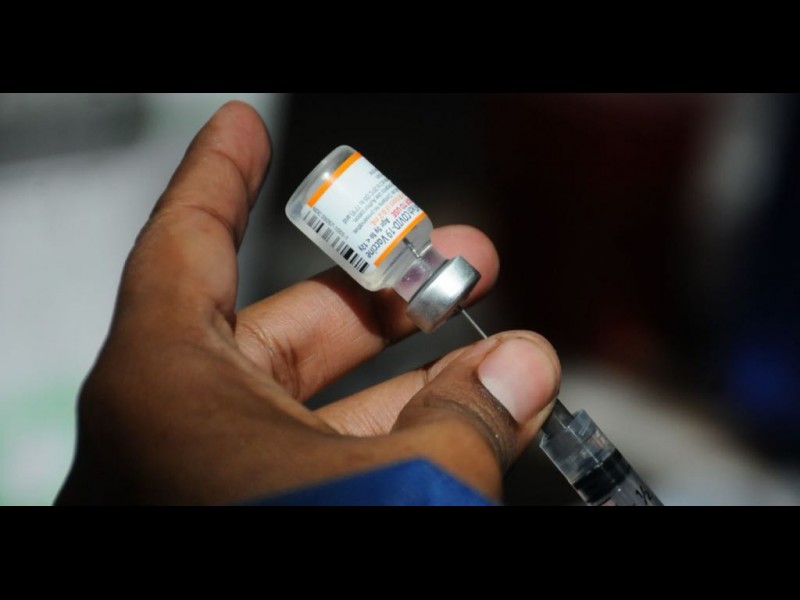
#Vacunas #Cofepris #C19
(Latinus). La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) informó que recibió solicitudes de empresas farmacéuticas para obtener el registro sanitario de cuatro vacunas contra la Covid-19 para su comercialización en el país.
A través de un comunicado, la Cofepris informó que las vacunas son la Comirnaty, de Pfizer S.A. de C.V.; Vaxzevria, de AstraZeneca S.A. de C.V.; así como Spikevax y Spikevax bivalente, de ModernaTx Inc.
Estas farmacéuticas presentaron las solicitudes luego de que el 22 de septiembre el regulador lanzó la convocatoria para la comercialización de las vacunas
Asimismo, señaló que Comirnaty de Pfizer será la primera vacuna en ser evaluada por Comité de Moléculas Nuevas (CMN), como parte del proceso de transición de la autorización de uso de emergencia hacia el registro sanitario.
“A través de este proceso regulatorio, pionero en el mundo, Cofepris refrenda su compromiso de ser una autoridad sanitaria ágil, justa y transparente, enfocada en proteger la salud y garantizar el acceso sanitario con altos estándares de calidad”, indicó el regulador.
Posteriormente, será evaluada Vaxzevria de AstraZeneca, y por último Spikevax y Spikevax bivalente de ModernaTx, a través de su representante legal en México, Asofarma S.A. de C.V.
“Es importante mencionar que el CMN es la instancia de consulta que emite la opinión técnica sobre la seguridad, calidad y eficacia de diferentes insumos para la salud. Sin embargo, estas opiniones no son vinculantes para la autorización final otorgada por Cofepris”, apuntó.
La Cofepris señaló en la convocatoria que antes de obtener su registro sanitario, las empresas deberán comprobar la calidad, seguridad y eficacia de los productos, los cuales serán evaluados por personal dictaminador especializado en medicamentos biológicos y biotecnológicos.
Señaló que las empresas deberán abstenerse de cualquier intento de interferir directa o indirectamente en la evaluación del producto farmacéutico y advirtió que toda actividad irregular será denunciada ante la Secretaría de la Función Pública (SFP).
Nota original
LATINUS



